- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:47.
- Última modificação 2025-06-01 07:37.
A principal diferença entre ácido carbônico e bicarbonato é que o ácido carbônico é um composto químico neutro, enquanto o bicarbonato é um composto químico carregado negativamente.
O ácido carbônico é um ácido fraco que se forma em solução quando o dióxido de carbono se dissolve em água, com a fórmula química H2CO3. O bicarbonato se forma pela combinação de três átomos de oxigênio, um átomo de hidrogênio e um átomo de carbono com a fórmula química HCO3-.
O que é ácido carbônico?
O ácido carbônico é H2CO3. Às vezes, damos esse nome a soluções com dióxido de carbono dissolvido em água ou água gaseificada. Isso ocorre porque a água carbonatada contém uma pequena quantidade de H2CO3. Além disso, o ácido carbônico é um ácido fraco e pode formar dois tipos de sais como carbonatos e bicarbonatos. A massa molar deste composto é 62,024 g/mol.
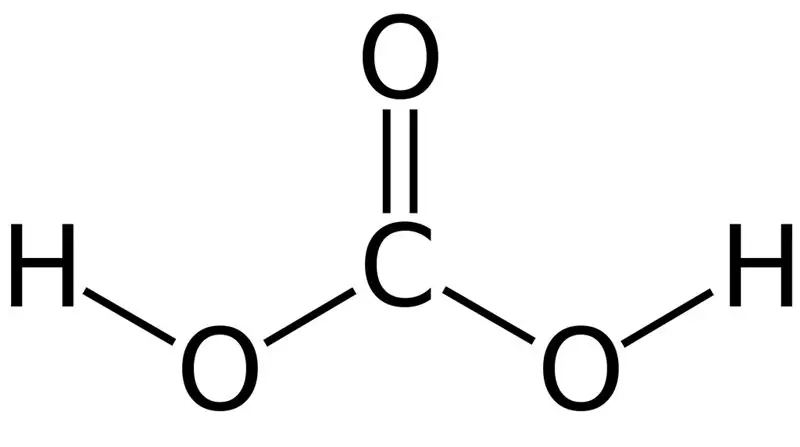
Figura 01: A Estrutura Química do Ácido Carbônico
Quando o dióxido de carbono se dissolve na água, ele entra em equilíbrio entre o dióxido de carbono e o ácido carbônico. O equilíbrio é o seguinte:
CO2 + H2O ⟷ H2CO3
Se adicionarmos um excesso de ácido carbônico a uma base, resulta em bicarbonato. Mas, se houver um excesso de base, o ácido carbônico tende a dar sais carbonatados. Mais precisamente, o ácido carbônico é um composto de ácido carboxílico que possui dois substituintes de grupo hidroxila ligados ao carbono carbonílico. Além disso, é um ácido poliprótico, capaz de doar prótons. Possui dois prótons removíveis, portanto é especificamente diprótico.
O que é bicarbonato?
O bicarbonato se forma pela combinação de três átomos de oxigênio, um átomo de hidrogênio e um átomo de carbono. O produto dessa combinação pode ser um íon ou um composto com mais elétrons do que prótons. Podemos descrevê-lo como uma espécie química com a fórmula química HCO3-.
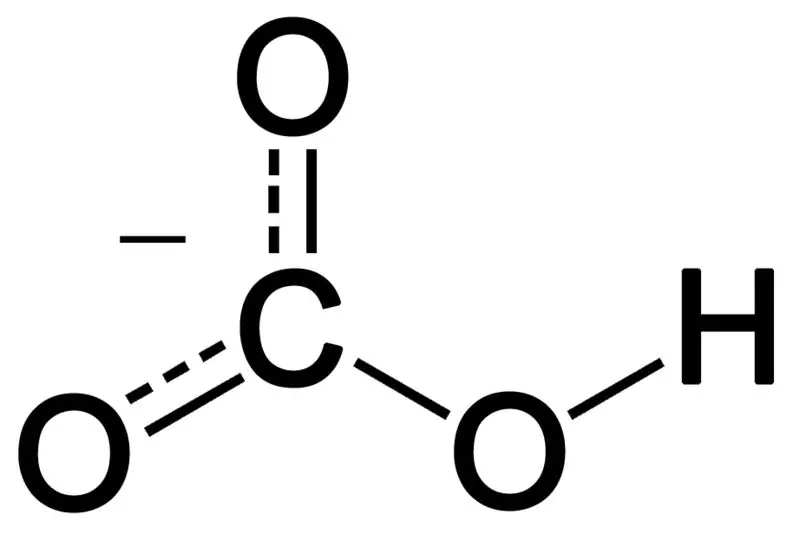
Figura 02: A estrutura química do ânion bicarbonato
Este composto é uma parte crucial do sistema de tamponamento de pH do corpo, em termos leigos: é responsável por manter o sangue em um estado que não seja muito ácido ou muito básico. Além disso, serve como uma maneira de manter os sucos digestivos sob controle quando o estômago termina de digerir os alimentos. Além disso, o ácido carbônico na água da chuva forma íons de bicarbonato quando atinge as rochas. Este fluxo de íons bicarbonato é importante para manter o ciclo do carbono funcionando.
Qual é a diferença entre ácido carbônico e bicarbonato?
O ácido carbônico é um ácido fraco que se forma em solução quando o dióxido de carbono se dissolve em água, e sua fórmula química é H2CO3. O bicarbonato se forma pela combinação de três átomos de oxigênio, um átomo de hidrogênio e um átomo de carbono com a fórmula química HCO3-. A principal diferença entre o ácido carbônico e o bicarbonato é que o ácido carbônico é um composto químico neutro, enquanto o bicarbonato é um composto químico carregado negativamente. Além disso, o ácido carbônico é usado para fazer espumantes, refrigerantes, tratar dermatites, enxaguatórios bucais, etc.
O infográfico a seguir resume a diferença entre ácido carbônico e bicarbonato em forma de tabela para comparação lado a lado.
Resumo - Ácido carbônico vs bicarbonato
O ácido carbônico é H2CO3. O bicarbonato se forma pela combinação de três átomos de oxigênio, um átomo de hidrogênio e um átomo de carbono, com a fórmula química HCO3-. A principal diferença entre o ácido carbônico e o bicarbonato é que o ácido carbônico é um composto químico neutro, enquanto o bicarbonato é um composto químico carregado negativamente.






